Đa u tủy xương là một bệnh lý ác tính nguy hiểm gây ra rất nhiều biến chứng. Ở giai đoạn đầu, bệnh rất khó phát hiện do có thể không gây ra bất cứ triệu chứng nào. Trường hợp gặp phải các triệu chứng nghi ngờ mắc bệnh cần sớm thăm khám để được bác sĩ chẩn đoán xác định bệnh và có phương pháp điều trị phù hợp.
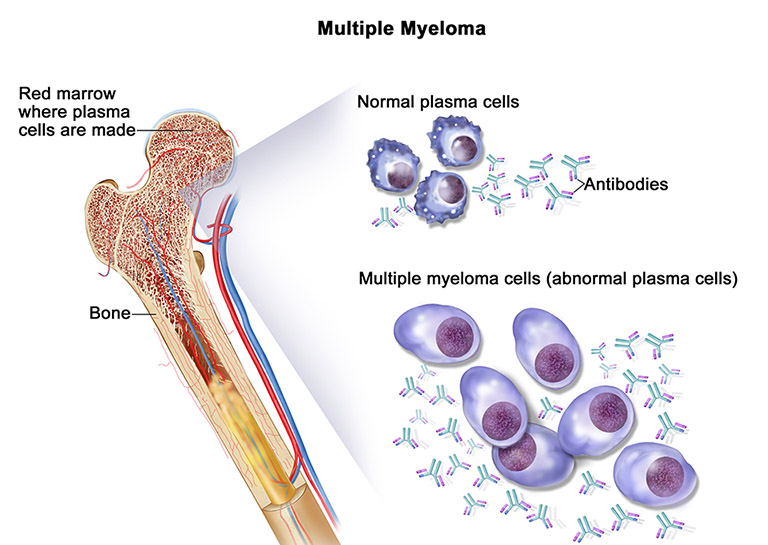
Đa u tủy xương là bệnh gì?
Đa u tủy xương (Multiple Myeloma) là một bệnh ung thư huyết học nguy hiểm. Bệnh đặc trưng bởi sự tăng sinh ác tính của các tế bào dòng plasmo tiết ra protein đơn dòng trong máu và nước tiểu.
Ở bệnh lý này, các tế bào huyết tương ung thư sẽ tích tụ bên trong tủy xương và lấn ác các tế bào máu khỏe mạnh. Thay vì tạo ra các kháng thể hữu ích thì các tế bào ung thư lại tạo ra các protein bất thường. Từ đó có thể gây ra các biến chứng.
1. Nguyên nhân gây bệnh
Hiện nay, nguyên nhân gây bệnh đa u tủy xương vẫn chưa được xác định rõ ràng. Các chuyên gia cho biết, bệnh lý này bắt đầu từ 1 tế bào huyết tương bất thường ở bên trong tủy xương. Tế bào này có tốc độ nhân lên rất nhanh chóng.
Các tế bào ung thư sẽ không chết đi mà tích tụ lại, lấn át quá trình sản sinh các tế bào khỏe mạnh. Cụ thể là ở bên trong tủy xương, các tế bào ác tính sẽ gây chèn ép các tế bào máu khỏe mạnh. Từ đó khiến cơ thể mệt mỏi và không có khả năng chống lại nhiễm trùng.
Dưới đây là các yếu tố có thể làm tăng nguy cơ bị đa u tủy xương:
- Tuổi cao: Thực tế, tuổi càng cao thì nguy cơ mắc bệnh đa u tủy xương càng tăng lên. Hầu hết người bệnh được chẩn đoán ở độ tuổi giữa 60.
- Giới tính: Số liệu thống kê cho thấy, nam giới có nguy cơ mắc bệnh lý này cao hơn nữ giới.
- Chủng tộc: Người da đen có nhiều khả năng mắc bệnh đa u tủy xương hơn là những người thuộc các chủng tộc khác.
- Tiền sử bệnh lý của gia đình: Nếu có người thân cận huyết mắc bệnh thì nguy cơ bị đa u tủy xương của bạn cũng sẽ cao hơn những đối tượng bình thường khác.
- Tiền sử cá nhân về bệnh MGUS (bệnh gammopathy đơn dòng có ý nghĩa chưa xác định): Đa u tủy xương hầu hết khởi phát dưới dạng MGUS. Chính vì vậy mà tình trạng này được cho là sẽ làm tăng nguy cơ mắc bệnh.
2. Triệu chứng
Trong giai đoạn đầu, bệnh đa u tủy xương có thể không gây ra bất cứ triệu chứng lâm sàng nào. Trường hợp bệnh đã tiến triển thì triệu chứng có thể khác nhau ở từng cá thể người bệnh.
Dưới đây là một số triệu chứng có thể bắt gặp:
- Đau xương, nhất là vùng cột sống và vùng ngực
- Buồn nôn
- Ăn không ngon miệng
- Táo bón
- Tinh thần mệt mỏi, hoang mang
- Nhiễm trùng thường xuyên
- Yếu hoặc tê chân
- Thường xuyên cảm thấy khát
- Giảm cân
Nên sớm tìm gặp bác sĩ nếu có các dấu hiệu và triệu chứng kéo dài dai dẳng khiến cho bạn cảm thấy lo lắng, bất an.
Bệnh đa u tủy xương có nguy hiểm không?
Đa u tủy xương được đánh giá là một bệnh lý nguy hiểm. Bệnh có thể gây ra nhiều biến chứng nghiêm trọng. Thậm chí còn đe dọa cả tính mạng.
Một số biến chứng thường gặp của bệnh bao gồm:
- Suy thận
- Nhiễm khuẩn phổi
- Nhiễm khuẩn đường tiết niệu
- Biến chứng thần kinh do chèn ép tủy
- Suy tủy
- Chảy máu
- Tăng acid uric máu do hóa trị liệu
Tiên lượng sống của bệnh còn phụ thuộc vào rất nhiều yếu tố liên quan. Điển hình như phát hiện bệnh sớm hay muộn, khả năng đáp ứng điều trị của từng cá thể người bệnh, thể trạng sức khỏe, điều kiện chăm sóc… Nhiều trường hợp, bệnh có thể gây tử vong nhanh chóng sau khi chỉ mới phát hiện bệnh không lâu.
Chẩn đoán bệnh đa u tủy xương
Để đưa ra chẩn đoán xác định bệnh đa u tủy xương, bác sĩ cần căn cứ vào kết quả chẩn đoán lâm sàng và chẩn đoán cận lâm sàng để đối chiếu trên tiêu chuẩn chẩn đoán. Ngoài ra, trong một số trường hợp, việc thực hiện chẩn đoán phân biệt có thể cần thiết.

1. Chẩn đoán lâm sàng
Chẩn đoán lâm sàng bệnh đa u tủy xương bao gồm:
- Thiếu máu: Có khoảng 70% người bệnh mới có xuất hiện tình trạng thiếu máu.
- Tổn thương xương: Khoảng 60% người bệnh mới gặp phải. Biểu hiện gồm đau xương, u xương và gãy xương.
- Suy thận: Chiếm khoảng 20%. Trong đó có khoảng 10% người bệnh mới được chẩn đoán có suy phận nặng và cần thực hiện chạy thận nhân tạo.
- Tăng calci máu: Các biểu hiện thường gặp là buồn nôn, táo bón, suy thận…
- Nhiễm trùng: Phát hiện nhiễm trùng tái diễn.
- Bệnh lý tổn thương: Có 3 loại tổn thương phổ biến bao gồm thâm nhiễm thần kinh trung ương, bệnh lý thần kinh ngoại biên và chèn ép rễ – tủy sống.
- Tăng độ quánh máu: Biểu hiện thường gặp là khó thở, chảy máu mũi, xuất huyết võng mạc…
2. Chẩn đoán cận lâm sàng
Các xét nghiệm cận lâm sàng được chỉ định trong chẩn đoán đa u tủy xương có thể bao gồm:
– Xét nghiệm tủy xương:
- Phát hiện tăng tỷ lệ tế bào dòng plasmo. Bên cạnh đó còn có thể thấy giảm tạo cốt bào, tăng hủy cốt bào, hình ảnh rối loạn sinh tủy thứ phát…
- Xét nghiệm lai huỳnh quang tại chỗ (fluorescence in situ hybridization: FISH): Phát hiện ra các tổn thương bao gồm t(11;14), t(6;14), t(4;14), t(14;16), del 13; del 17…
- Phân tích dấu ấn miễn dịch (immunophenotypic): Điển hình là CD56+, CD138+, có khoảng 20% có CD20+.
- Ngoài ra còn có thể thực hiện sinh thiết mô, chẩn đoán u tương bào khi có u, nhuộm hóa mô miễn dịch.
– Điện di protein huyết thanh và nước tiểu:
Xét nghiệm này sẽ giúp phát hiện protein đơn dòng. Ngoài ra điện di miễn dịch còn phát hiện thành phần đơn dòng của các chuỗi nhẹ và nặng.
– Xét nghiệm sinh hoá:
- Có thể có: Giảm albumin; tăng protid máu toàn phần; tăng globulin, creatinine, β2-microglobulin và canxi huyết thanh.
- Định lượng globulin miễn dịch IgG, IgA, IgM kết hợp do chuỗi nhẹ tự do trong nước tiểu và huyết thanh.
- Ngoài ra còn thực hiện xét nghiệm protein Bence-Jone để định lượng protein nước tiểu/ 24h.
– Xét nghiệm hình ảnh:
- Chụp X-quang xương (xương chậu, cột sống, xương sườn, xương sọ…): Có phát hiện tổn thương tiêu xương.
- Chụp cộng hưởng từ (MRI) hoặc chụp cắt lớp vi tính (CT Scan): Có thể sẽ cần thiết trong các trường hợp xuất hiện triệu chứng đau xương nhưng khi chụp X-quang lại không phát hiện tổn thương.
- Chụp PET/CT hoặc PET/MRI: Giúp phát hiện các tổn thương mới, bao gồm cả tổn thương ngoài tủy và chèn ép tủy sống.
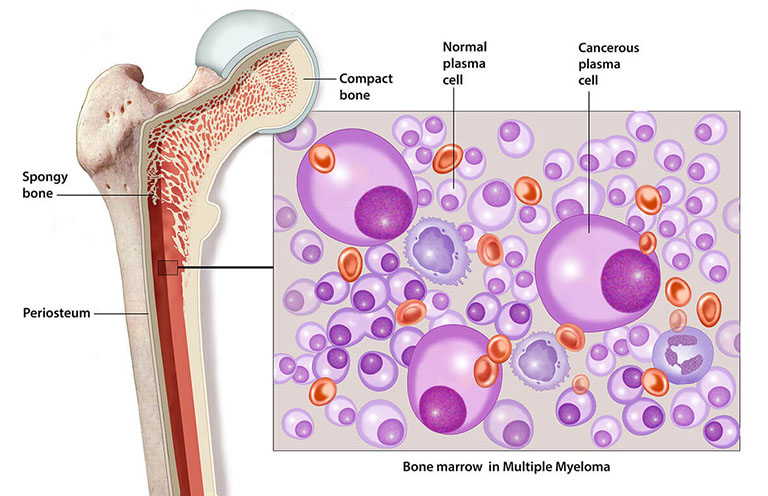
3. Tiêu chuẩn chẩn đoán
Các xét nghiệm kể trên có thể giúp chẩn đoán các thể bệnh Đa u tủy xương bao gồm:
– Bệnh lý gamma đơn dòng có ý nghĩa không xác định (MGUS: monoclonal gammopathy of undetermined significance ):
Có tất cả 3 tiêu chuẩn sau:
- Protein đơn dòng trong huyết thanh ở mức dưới 3g/dL.
- Tế bào dòng plasmo ở trong tủy xương dưới 10%.
- Không phát hiện tổn thương cơ quan (suy thận, thiếu máu, tăng calci máu và tổn thương xương)
– Đa u tủy xương tiềm tàng (SMM: smouldering multiple myeloma):
Được xác định khi có cả 2 tiêu chuẩn sau:
- Protein đơn dòng trong huyết thanh (IgG hoặc IgA) ở mức từ 3g/dL trở lên. Hoặc các tế bào dòng plasmo trong tủy xương ở mức từ 10% trở lên.
- Không phát hiện tổn thương cơ quan (suy thận, thiếu máu, tăng calci máu và tổn thương xương).
– Đa u tủy xương có triệu chứng (MM: multiple myeloma):
Được xác định khi có tất cả các tiêu chuẩn sau:
- Tế bào dòng plasmo trong tủy xương ở mức từ 10% trở nên hoặc sinh thiết chứng minh là có u tế bào dòng plasmo.
- Tăng calci máu trên 11.5mg/dL.
- Suy thận: Creatinine huyết thanh trên 1.73mmol/L (hoặc trên 2mg/dL) hoặc độ thanh thải creatinin ước tính dưới 40ml/phút.
- Thiếu máu: Bình sắc, hồng cầu bình thường với hemoglobin dưới 2g/dL thấp hơn mức giới hạn bình thường hoặc hemoglobin dưới 10g/dL.
- Tổn thương xương: Tiêu xương nặng, loãng xương hoặc gãy xương bệnh lý.
4. Chẩn đoán phân biệt
Bệnh đa u tủy xương có thể cần được chẩn đoán phân biệt với một số bệnh lý sau:
- U tế bào dòng plasmo ngoài tuỷ: Đặc trưng là sự tăng sinh tế bào dòng plasmo được thể hiện trên sinh thiết tổn thương ở xương hoặc phần mềm. Không phát hiện bằng chứng của tăng sinh tế bào dòng plasmo ở trong tủy xương trên sinh thiết và tủy đồ.
- Bệnh Waldenstrom: Biểu hiện cụ thể là tăng sinh lympho, tăng IgM trên 3g/dL. Đồng thời có sự xuất hiện của các tế bào lympho dạng tế bào dòng plasmo trong tủy xương.
- Lơ xê mi tế bào dòng plasmo: Có thể ở dạng nguyên phát hoặc thứ phát sau đa u tủy xương. Bệnh lý này được chẩn đoán khi máu ngoại vi có chứa tỷ lệ tế bào dòng plasmo trên 20% hoặc số lượng tuyệt đối trên 2G/L.
Các phương pháp điều trị bệnh đa u tủy xương
Điều trị đa u tủy xương không phải lúc nào cũng cần thiết ngay lập tức. Trường hợp bệnh phát triển chậm và không gây ra triệu chứng thì bác sĩ có thể để nghị theo dõi chặt chẽ.
Còn đối với các trường hợp người bệnh đa u tủy xương cần điều trị thì một số phương pháp dưới đây có thể giúp kiểm soát bệnh:
1. Điều trị ban đầu
Người bệnh bị đa u tủy xương tiềm tàng thường không có chỉ định điều trị ngay. Cần căn cứ vào khả năng có thể thực hiện được việc ghép tế bào gốc tự thân cho từng ca bệnh hay không để lựa chọn các phác đồ điều trị cho phù hợp và hiệu quả.

– Người bệnh không có chỉ định ghép tế bào gốc:
Thường là những người bệnh trên 65 tuổi và có thể trạng bệnh kém. Trong đó thể trạng bệnh có nghĩa lớn hơn so với tuổi của người bệnh trong lựa chọn ghép tế bào gốc tự thân. Với các trường hợp không có chỉ định tế bào gốc thì bác sĩ có thể yêu cầu điều trị bằng một số phác đồ sau:
+ MP: Melphalan và Methylprednisone:
Phác đồ này được thực hiện 12 đợt, cứ 4 – 6 tuần sẽ thực hiện 1 đợt điều trị. Bác sĩ sẽ dựa vào số lượng tiểu cầu và bạch cầu để điều chỉnh liều Melphalan.
+ MPT: Melphalan + methylprednisone + thalidomide:
- Melphalan: Sử dụng với liều 0,25mg/kg or 4mg/m2/ngày theo đường uống, ngày dùng 1 – 4.
- Methylprednisone: Dùng với liều 2mg/kg/ngày theo đường uống, ngày dùng 1 – 4.
- Thalidomide: Dùng liều 100 – 400mg/ngày theo đường uống, dùng liên tục.
MP: Dùng 12 đợt (cách 4 – 6 tuần/ đợt). Điều chỉnh liều melphalan theo số lượng tiểu cầu và bạch cầu. Còn Thalidomide dùng kéo dài 72 tuần.
+ VMP: Bortezomib + melphalan + methylprednisone:
- Melphalan: Dùng liều 9mg/m2/ngày theo đường uống, ngày dùng 1 – 4.
- Methylprednisone: Dùng với liều 60mg/m2/ngày theo đường uống, ngày dùng 1 – 4.
- Bortezomib: Dùng liều 1,3mg/m2 bằng cách tiêm dưới da hoặc tiêm tĩnh mạch. Đợt đầu dùng các ngày 1, 4, 8, 11. Đợt tiếp dùng các ngày 1, 8, 15, 22.
Cách 5 tuần dùng 1 đợt x 8 đợt. Lenalidomide dùng kết hợp với dexamethasone liều thấp. Còn Bendamustine dùng kết hợp với methylprednisone (chỉ định cho người bệnh không thể ghép tủy và có các biểu hiện thần kinh ngoại biên chống chỉ định với điều trị ị bortezomib và thalidomide).
– Người bệnh có khả năng ghép tế bào gốc tự thân:
Thường là những người bệnh dưới 65 tuổi và có tình trạng lâm sàng tốt. Việc điều trị sẽ được tiến hành như sau:
+ Điều trị tấn công:
Dưới đây là các phác đồ cụ thể theo thứ tự ưu tiên:
+ VTD: Bortezomib + Thalidomide + Dexamethasone:
- Bortezomib: Dùng liều 1,3 mg/m2 bằng cách tiêm dưới da hoặc tiêm tĩnh mạch. Đợt đầu dùng các ngày 1, 4, 8, 11. Đợt tiếp theo dùng các ngày 1, 8, 15, 22.
- Thalidomide: Dùng liều 100 – 200mg theo đường uống. Dùng liên tục.
- Dexamethasone: Dùng liều 40mg/ngày theo đường uống, ngày dùng 1 – 4.
+ VCD: Bortezomib + Cyclophosphamide + Dexamethasone:
- Bortezomib: Dùng liều 1,3 mg/m2 bằng cách tiêm dưới da hoặc tiêm tĩnh mạch. Đợt đầu dùng các ngày 1, 4, 8, 11. Đợt tiếp theo dùng các ngày 1, 8, 15, 22.
- Cyclophosphamide: Dùng liều 300mg/m2/ngày bằng cách truyền tĩnh mạch. Dùng các ngày 1, 8, 15, 22.
- Dexamethasone: Dùng liều 40mg/ngày bằng cách truyền tĩnh mạch. Dùng ngày 1 – 4.
Ngoài ra, bác sĩ có thể chỉ định một số phác đồ khác trong giai đoạn điều trị tấn công. Ví dụ như PAD (Bortezomib + Doxorubicin + Dexamethasone) hoặc VRD (Bortezomib + Lenalidomide + Dexamethasone).
+ Điều trị ghép tế bào gốc tự thân:
Sau khi đã điều trị tấn công đạt lui bệnh một phần hoặc lui bệnh hoàn toàn, bác sĩ sẽ lựa chọn những người bệnh chưa điều trị bằng các thuốc có ảnh hưởng tới tế bào gốc như melphalan để tiến hành điều trị ghép tế bào gốc tự thân.
Các bước trong ghép tế bào gốc tự thân bao gồm:
- Lựa chọn nguồn tế bào gốc: Có thể lựa chọn từ tủy xương hoặc máu ngoại vi. Tuy nhiên đa số sử dụng nguồn tế bào gốc từ máu ngoại vi.
- Huy động, thu gom và lưu trữ bảo quản tế bào gốc từ máu ngoại vi.
- Điều kiện hóa cho người bệnh: Dùng melphalan liều 200mg/m2 da, truyền tĩnh mạch trong 1 giờ.
- Quy trình truyền tế bào gốc: Tiến hành truyền sau khi đã kết thúc điều kiện hóa 24 giờ. Nếu truyền tươi tế bào gốc từ tủy xương hay máu ngoại vi: Tốc độ truyền 40 – 50 giọt/ phút. Nếu truyền tế bào gốc bảo quản âm sâu: Cần truyền càng nhanh càng tốt sau khi rã đông.
- Cuối cùng cần dự phòng biến chứng và các phản ứng bằng cách sử dụng methylprednisolon và thuốc kháng histamin.
+ Điều trị duy trì:
- Trường hợp sau ghép không đẩy lùi được bệnh: Cần điều trị duy trì lenalidomide.
- Trường hợp sau ghép đẩy lùi được bệnh: Điều trị duy trì với thalidomide liều 100 mg/ngày trong 2 năm.
- Trường hợp người bệnh thuộc nhóm nguy cơ cao: Cần điều trị duy trì bằng phác đồ có bortezomib với liều 1,3 mg/m2 mỗi 2 tuần trong 2 năm.
2. Điều trị bệnh tái phát và kháng thuốc
Trong một số trường hợp, người bệnh có thể bị kháng thuốc hay bệnh tái phát. Lúc này điều trị có thể bao gồm:
- Phác đồ dexamethasone kết hợp với lenalidomide.
- Kết hợp các bộ ba như VCD, VTD… cho các trường hợp tái phát sau khi ghép tế bào gốc tự thân.
- Phác đồ pegylated liposomal doxorubicin (PLD) kết hợp bortezomib.
- Ở những người bệnh trẻ tuổi bị tái phát, có thể chỉ định ghép tế bào gốc tự thân lần 2.
3. Điều trị hỗ trợ
Tùy thuộc vào mức độ ảnh hưởng của bệnh mà bác sĩ sẽ yêu cầu các giải pháp điều trị hỗ trợ khác nhau. Có thể bao gồm:
– Điều trị suy thận:
- Nên điều trị theo phác đồ có bortezomib và không cần thiết phải điều chỉnh liều bortezomib. Bác sĩ có thể yêu cầu kết hợp lenalidomide và dexamethasone.
- Chăm sóc chức năng thận: Cần giảm acid uric, giảm canxi. Đồng thời có thể trao đổi huyết tương.
- Phòng suy thận: Cần hạn chế thuốc chống viêm non-steroid, kháng sinh nhóm aminoglycoside.
– Điều trị thiếu máu:
- Erythropoietin tái tổ hợp thường được chỉ định. Có thể dùng liều 4.000 UI/ ngày hoặc thay thế bằng liều 10.000UI/ 1 lần x 3 lần/ tuần. Mục đích là để giúp huyết sắc tố đạt trên 12G/L.
- Ngoài ra bác sĩ có thể yêu cầu truyền khối hồng cầu.
– Trường hợp có tổn thương xương:
- Điều trị tăng canxi máu: Cần truyền dịch hoặc uống thuốc lợi tiểu. Kết hợp dùng các thuốc ức chế hủy xương như Bisphosphonate, solumedrol (50-100mg/ngày), calcitonine (4-8 UI/kg pha NaCl 0,9% truyền trong 6-8 giờ). Ngoài ra lọc máu có thể được chỉ định khi tăng canxi máu đe dọa đến tính mạnh, có phù phổi, suy thận.
- Sử dụng Bisphosphonate: Có thể dùng Zoledronic acid với liều 4mg/ lần/ tháng (nếu có suy thận thì phải giảm liều). Hoặc dùng Pamidronate với liều 90mg/ tháng, truyền tĩnh mạch trong 2 giờ.
- Trường hợp đau nhiều: Bác sĩ có thể chỉ định tia xạ nếu cơn đau có tính khu trú.
– Đối với nhiễm trùng:
- Có thể dùng gammaglobulin để phòng nhiễm trùng.
- Trường hợp có nhiễm trùng xuất hiện thì phải điều trị bằng kháng sinh ngay.
– Trường hợp tổn thương hệ thống thần kinh:
- Thâm nhiễm thần kinh trung ương: Bác sĩ có thể chỉ định tia xạ, tiêm tủy sống và điều trị toàn thân.
- Éo tủy: Được điều trị bằng Dexamethasone liều cao. Ban đầu là 100mg, sau đó là 25mg cho mỗi 6 giờ rồi giảm dần liều. Tia xạ tại chỗ càng sớm càng tốt và kết hợp đồng thời dexamethasone liều cao.
– Điều trị tăng độ quánh máu.
Cần trao đổi huyết tương khi phát hiện các biểu hiện của tăng độ quánh máu. Điển hình như chảy máu niêm mạc, đau đầu, chóng mắt, co giật, hôn mê hoặc độ quánh máu tăng trên 4 centipoise.
Đa u tủy xương là bệnh lý nguy hiểm cần sớm phát hiện và tích cực điều trị. Cần tuyệt đối tuân thủ phác đồ mà bác sĩ đưa ra. Nên giữ tinh thần lạc quan để tránh làm ảnh hưởng đến quá trình kiểm soát bệnh của các phương pháp điều trị.
Có thể bạn quan tâm:
The post Đa u tủy xương là gì? Có chữa được không? appeared first on TRUNG TÂM NGHIÊN CỨU VÀ ỨNG DỤNG THUỐC DÂN TỘC.
Xem các khuyến mãi của Concung.com:
[atcoupon type="concung"]




0 Nhận xét
Đăng nhận xét